癌癥免疫治療的核心在于激活人體自身的免疫系統(tǒng)來識別和殺滅腫瘤細(xì)胞,而樹突狀細(xì)胞(DC)作為最重要的專職抗原呈遞細(xì)胞,能夠有效介導(dǎo)固有免疫應(yīng)答并激活適應(yīng)性免疫,其功能狀態(tài)還決定了免疫應(yīng)答的強(qiáng)度與質(zhì)量,因而在抗腫瘤免疫中處于核心地位。近年來研究發(fā)現(xiàn),NLRP3炎性小體的激活可以誘導(dǎo)DC進(jìn)入一種"超激活"的特殊狀態(tài),超激活DC不同于NLRP3激活通常導(dǎo)致的細(xì)胞焦亡,能夠在分泌白細(xì)胞介素-1β的同時保持細(xì)胞活力,并上調(diào)共刺激分子表達(dá),兼具更高效的抗原呈遞能力和更強(qiáng)的遷移能力,是促進(jìn)CD8+ T細(xì)胞免疫應(yīng)答的理想DC表型。然而,目前的DC超激活誘導(dǎo)方案仍普遍存在啟動信號安全性不足、激活信號組成復(fù)雜、刺激強(qiáng)度難以調(diào)控等問題,從而限制了其在腫瘤疫苗中的進(jìn)一步應(yīng)用。
針對以上問題,中國科學(xué)院上海硅酸鹽研究所陳航榕研究員、馬明研究員團(tuán)隊構(gòu)建了脂肪酸修飾并負(fù)載質(zhì)粒DNA(pDNA)的脂質(zhì)納米顆粒(FA-pLNP)平臺。其中,pDNA可編碼腫瘤抗原并提供NF-κB介導(dǎo)的NLRP3炎癥小體啟動信號;脂肪酸提供炎癥小體的激活信號,并通過調(diào)節(jié)信號強(qiáng)度實現(xiàn)了對DC超激活狀態(tài)的可控誘導(dǎo)。相關(guān)成果以"Combinatorial Design of Fatty Acid-Incorporated Plasmid Lipid Nanoparticles Drives Dendritic Cell Hyperactivation for Enhanced Cancer Immunotherapy"為題發(fā)表在《ACS Nano》上。
本研究以FDA批準(zhǔn)的疫苗脂質(zhì)組成與比例作為基準(zhǔn)配方,引入四種不同碳鏈長度及飽和度的脂肪酸,分別按五個摩爾比梯度摻入,構(gòu)建了包含20種候選配方的FA-pLNP庫。以DC成熟度為篩選指標(biāo),最終篩選得到最優(yōu)配方——摻入15%棕櫚酸的pLNP(命名為PA15)。
本研究基于團(tuán)隊自主開發(fā)的螺旋聚焦流微混合器,實現(xiàn)了優(yōu)選脂質(zhì)納米顆粒PA15的穩(wěn)定可控制備。該微混合器采用摩方精密面投影微立體光刻(PμSL)3D打印技術(shù)(nanoArch? S140,精度:10 μm),一體化成型出具有3D同軸聚焦螺旋通道的復(fù)雜結(jié)構(gòu)。含有脂質(zhì)的乙醇溶液與含pDNA的水溶液分別從獨立入口注入,在螺旋通道內(nèi)流動并進(jìn)入混合區(qū),兩相流體快速混合,促使脂質(zhì)與pDNA在毫秒級時間內(nèi)完成自組裝,從而獲得粒徑更均一的納米顆粒。此外,團(tuán)隊以螺旋聚焦流微混合器為核心,開發(fā)了螺旋聚焦流納米藥物合成儀。該儀器配備觸屏數(shù)顯界面、微混合器連接件及自動收集臺,具有批次間高重復(fù)性、操作簡便等優(yōu)勢,適用于納米脂質(zhì)體、脂質(zhì)納米顆粒等多種納米顆粒的高流速、均一化合成。
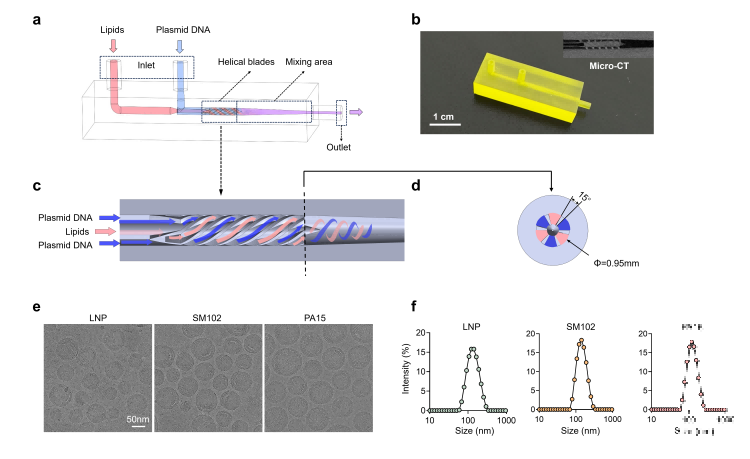
圖.(a)螺旋聚焦流微混合器裝置示意圖;(b)裝置實物照片及核心混合區(qū)的顯微CT圖像;(c)混合區(qū)內(nèi)流動模式示意圖;(d)螺旋通道出口處的橫截面視圖;(e)三種不同配方獲得的脂質(zhì)納米顆粒的冷凍透射電鏡圖像;(f)通過動態(tài)光散射測得不同類型脂質(zhì)納米顆粒的水合動力學(xué)粒徑分布。
進(jìn)一步研究證實,在B16-OVA和MC38兩種小鼠腫瘤模型中,PA15顯著增強(qiáng)DC成熟與抗原呈遞,能從數(shù)量(增加比例)、質(zhì)量(增強(qiáng)功能)和空間分布(促進(jìn)浸潤)三個維度全面誘導(dǎo)強(qiáng)效的CD8? T細(xì)胞應(yīng)答,腫瘤生長抑制率分別達(dá)到91.7%和74.1%。上述發(fā)現(xiàn)為癌癥疫苗及相關(guān)免疫治療的研究提供了新的思路。
上述研究成果系中國科學(xué)院上海硅酸鹽研究所與國科大杭州高等研究院的科研人員共同完成,研究生李孜印和賈福浩為共同第一作者,馬明研究員和陳航榕研究員為共同通訊作者。
原文鏈接:https://doi.org/10.1021/acsnano.6c01946